
تاسعة أساسي تلخيص كتاب العلوم الفيزيائية 9 اساسي : اليكم جميع ملخصات دروس العلوم الفيزيائية للسنة 9 من التعليم الاعدادي الثلاثي الاول والثاني والثالث كامل السنة للاسعانة بها في مناظرة النوفيام و حل فروض المراقبة والتاليفة كما يمكنكم استعمال محتوى هذا الموضوع للاجابة عن اسئلة الامتحاننات الوطنية و الفروض التاليفية و المراقبة في مادة الفيزياء للسنة التاسعة اساسي كما يمكنكم تحميل كتاب العلوم الفيزيائية تعليم تونس
عناوين الدروس الملخصة
الكهرمغناطيس,, ,التيّار الكهربائي المتغيّر مفهوم التيّار الكهربائي المتغيّر, التيّار المتناوب, خاصيات التيّار المتناوب الجيبي, الكهرباء المنزليّة الكهرباء المنزليّة,, الكهرباء الساكنة, التكهرب بالاحتكاك والتكهرب بالتماس, الشحنة الكهربائية,, المادة في الطبيعة, ,الذرة والاحتراق المحروقات , أنواعها ومصادرها واستعمالاتها, نقل المحروقات وتخزينها والحماية من مخاطرها, التفاعل الكيميائي, الذرّة, بنية الذرة, الرموز الكيميائية, رمز الذرّة والصيغ الكيميائيّة, معادلات التفاعلات الكيميائيّة, المحاليل الشاردية, ناقليّة المحاليل المائيّة للكهرباء, تأثير التركيز على ناقليّة المحلول الشاردي للكهربائي, الأنيونات والكتيونات, المحلول المائي الحامضي والمحلول المائي القلوي, قيس PH محلول, درجة حموضة محلول مائي حامضي, درجة قلويّة محلول مائي قلوي, المحلول المتعادل,, الضوء, تغيير مسار الضوء, انعكاس الضوء, المرآة المسطّحة, انكسار الضوء, الانكسار الحدّي والانعكاس الكلّي, تطبيقات لتغيّر مسار الضوء, الأضواء المرئيّة والضوء الأبيض,, الطاقة الضوئيّة, مفهوم الطاقة الضوئية, الطاقة الشمسية,
والآن اليكم ملخص جميع دروس مادة الفيزياء للسنة التاسعة اساسي
الكهرمغناطيس
مفهوم التيّار الكهربائي المتغيّر
التيّار الكهربائي المتغيّر :
التيّار الكهربائي الثابت في اتجاهه (اتّجاه وحيد) وفي شدّته بمرور الزّمن هو تيّار كهربائي مستمرّ، أمّا التيّار الكهربائي غير الثابت في اتجاهه أو في شدّته بمرور الزّمن، فهو تيّار كهربائي متغيّر، وكلّ تيّار كهربائي غير مستمر هو تيّار متغيّر .
التوتّر الكهربائي المتغيّر :
إذا كان التوتّر الكهربائي المستمرّ هو التوتّر الثابت في قيمته الجبريّة بمرور الزمن، والذي نرمز له بالحرف U
، فإنّ التوتّر الكهربائي المتغيّر هو التوتّر غير الثابت في قيمته الجبريّة بمرور الزمن، والذي نرمز له بالحرف u
.
مولّدات التوتّر المتغيّر :
تُنعت المُولّدات التي تحفظ بين قطبيها توتّرا مستمرّا بمولّدات توتّر مستمرّ. أمّا المولّدات التي تحفظ بين قطبيها توتّرا غير مستمرّ (أو متغيّرا) فتنعت بمولّدات توتّر متغيّر.
شدّة التيار الكهربائي المتغيّر :
نرمز لشدّة التيار الكهربائي المستمرّ بالحرف I
، ونرمز لشدّة التيار الكهربائي المتغيّر بالحرف i
.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
التوتّر المتناوب :
كلّ توتّر كهربائي متغيّر يتميّز بقيمة جبريّة تتغيّر بالتناوب مع الزمن بين سالبة وموجبة، يسمّى توتّرا كهربائيّا متناوبا.
التوتّر الكهربائي المتناوب في الدارة المغلقة يولّد تيّارا متناوبا.
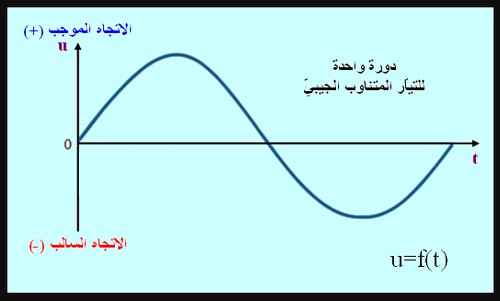
التوتّر المتناوب الجيبيّ :
التوتّر المتناوب الجيبيّا هو توتّر يتغيّر في شكل منحني جيبيّ. مثال : التوتّر الكهربائي المنزلي.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
خاصيات التيّار المتناوب الجيبي.
التيّار المتناوب الجيبي تيّار كهربائيّ دوريّ في التوتّر u
الذي يتولّد عنه وفي شدّته i
.
دورة التيّار المتناوب الجيبي T
هي المدّة الزمنيّة للتطوّر الجزئي الذي يتكرّر للتوتّر u
المتولّد عنه أو لشدّتهi
كما هو وبدون انقطاع، بينما التردّد N
هو عدد تلك التطوّرات الجزئيّة المتطابقة والمتتابعة في الثانية الواحدة.
N=
1T
مشواف الذبذبات جهاز عمليّ لإظهار الرسوم التذبذبيّة للتوتّرات الكهربائيّة المتناوبة ذات التردّد الذي لا يسمح بالمتابعة المباشرة لتطوّرها مع الزمن.
بالإضافة إلى دوريّته مع الزمن يتميّز التيّار المتناوب الجيبيّ بأنّ للتوتّر المتولّد عنه قيمة قصوى um
وقيمة فعّالة U
وبأنّ لشدّته قيمة قصوى im
وقيمة فعّالة I
.ـ
im=
I.2–√
um=
U.2–√
التوتّر الفعّال U
والشدّة الفعّالة I
للتيّار المتناوب الجيبيّ هما المقدران المساويان على التوالي لقيمة التوتّر المستمرّ U
ولقيمة شدّة التيّارالمستمرّ I
الذي يعطي للمصباح إشعاعا بنفس الشدّة.
بالنسبة إلى التيّار المتناوب الجيبيّ لا يقيس الفولتمتر إلاّ التوتّر الغعّال U
في حين أنّ الأمبيرمتر لا يقيس إلاّ الشدّة الفعّالة I
.
التوتّر الكهربائيّ المنزليّ في تونس هو توتّر متناوب جيبيّ ذو تردّد :
N=50Hz
وقيمة فعّالة :
U=220V
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الكهرباء المنزليّة
⇦ التوتّر الكهربائي المنزلي هو توتّر جيبي تردّده 50Hz وقيمته الفعّالة 220V.
⇦ توصل الشركة التونسيّة للكهرباء والغاز الكهرباء إلى المنازل عبر سلكين مختلفين هما سلك الطّور والسّلك المحايد. وسلك الطّور هو الذي يجعل مفكّ لوالب مختبار يشعّ.
⇦ حتى نتمكّن من تشغيل الأجهزة الكهربائيّة المنزليّة، نوصلها بسلكي الطّور والمحايد ونركبها بالتوازي.
⇦ يمكن للكهرباء المنزليّة أن تكون سببا في تعطلّ الأجهزة وذلك عندما تندلع الحرارة نتيجة لارتفاع شدّة التيّار الكهربائي الذي يعبر الأسلاك بقيمة لا تستطيع هذه الأخيرة تحمّلها. كما يمكنها أن تكون خطرة على الإنسان إذا أصابته بالصّعقة الكهربائيّة نتيجة لمرور التيار الكهربائيّ عبر جسمه.
⇦ تزداد خطورة الصّعقة الكهربائية كلّما ارتفعت شدّة التيّار الكهربائي الذي يعبر جسم الإنسان، لمرور التيّار الكهربائي عبره، وكلّما ارتفعت المدّة الزمنيّة التي تعرّض فيها الشخص للصّعقة.
هام:
⇦ تحدث الصّعقة الكهربائيّة إذا لامس شخص سلك الطّور والسّلك المحايد. أو لامس سلك الطّور والأرض.
⇦ لحماية الأشخاص تُوصل الهياكل المعدنيّة للأجهزة الكهربائيّة المنزليّة بسلك التأريض.
⇦ لضمان أكثر حماية للأشخاص والتجهيزات الكهربائيّة يُحبّذ تركيز فاصل تفاضلي في الجزء الرئيسي للشبكة الكهربائيّة ليلعب دور القاطع الآلي إذا تجاوزت قيمة شدّة التيّار الكهربائي المتسرّب عبر سلك التأريض قيمة 300mA.
⇦ لحماية الأجهزة، تُركّب في الشّبكات المنزليّة، الفواصل، والصهائر، لتقطّع مرور التيّار الكهربائي عن الأجهزة إذا تجاوزت شدّة التيار الكهربائي قيمة معيّنة.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الكهرباء الساكنة
التكهرب بالاحتكاك والتكهرب بالتماس.
⇦ تتغيّر خاصيّات المواد بتأثير الاحتكاك، حينها تصير قادرة على جذب الأجسام الخفيفة مثل قطع الورق الصغيرة أو الرّيش أو الشّعر. فنقول أنّ هذه المواد تكهربت. وتسمّى هذه الظاهرة بالتّكهرب، وتُنعتُ طريقة التّكهرب هذه بالتّكهرب بالاحتكاك.
⇦ يمكن أيضا كهربة الأجسام بالتّماس مع جسم آخر مكهرب.
⇦ كلّ جسم مكهرب يحمل كميّة من الكهرباء الساكنة.
⇦ النواس الكهربائي أداة كاشفة لظاهرة التكهرب.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الكهرباء الساكنة
أنواع الكهرباء
⇦ الكهرباء نوعان: كهرباء موجبة (أو زجاجيّة) مثل التي تظهر على مادّة الزّجاج المحكوك بالقطن، وكهرباء سالبة (أو راتنجية) مثل التي تظهر على قضيب إيبونيت محكوك بقطعة فراء.
⇦ يتنافر جسمان يحملان كهرباء من نفس النوع ويتجاذب جسمان يحملان كهرباء من نوعين مختلفين.
الشحنة الكهربائيّة
⇦ كلّ جسم مكهرب يحمل شحنة كهربائيّة رمزها q
.
⇦ الشحنة الكهربائيّة مقدار فيزيائي يُجسّم كمّية الكهرباء التي تظهر على جسم مكهرب.
⇦ الشّحنة الكهربائيّة مقدار قابل للقيس ووحدة قيسها الكولون ورمزها C
.
⇦ كلّ شحنة كهربائيّة لهما قيمة مطلقة مضاعفة لقيمة الشحنة الكهربائيّة البسيطة التي نرمز لها بـq
.
|q|=n×e
n∈N
وحيث
e=1,6.10−19C
خاصيّة التكهرب بالاحتكاك والتكهرب بالتماس
⇦ إذا تكهرب جسمان بالاحتكاك مع بعضهما فإنّهما يحملان كهرباء من نوعين مختلفين، أمّا إذا تكهرب جسم بالتماس مع جسم آخر مكهرب، فإنّ الجسمين يحملان كهرباء من نفس النوع.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المادّة في الطبيعة
الذرّة والاحتراق
المحروقات : أنواعها ومصادرها واستعمالاتها.
المحروقات هي المواد التي تنتج عند احتراقها طاقة حراريّة يمكن استغلالها في العديد من المجالات. وهي عديدة ومتنوّعة.
الحالات الفيزيائيّة للمحروقات
الحالة الصلبة :
توجد العديد من المحروقات على حالة فيزيائيّة صلبة، كالخشب والفحم والفحم الحجري.
الحالة السائلة :
توجد العديد من المحروقات على حالة فيزيائيّة سائلة، كالبنزين والمازوت والكحول.
الحالة الغازيّة :
توجد العديد من المحروقات على حالة فيزيائيّة غازيّة، كغاز البروبان وغاز الإيتان وغاز البوتان.
المصادر الطبيعيّة للمحروقات
من أهمّ مصادر المحروقات الطبيعيّة نذكر الأشجار وحقول النفط والغاز الطبيعي ومناجم الفحم الحجري.
استعمالات المحروقات
يمكن استغلال المحروقات في الصناعة والنقل والتدفئة والطبخ وغيرها… فالفحم مثلا نستعمله في منازلنا لنحصل على نار للتدفئة أو للطبخ، والبنزين والمازوت نستعملهما كوقود لسياراتنا والكيروسين يستعمل كوقود للطائرات والبرافين يستعمل لصناعة الشمع ولتشحيم الآلات…
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المادّة في الطبيعة
الذرّة والاحتراق
نقل المحروقات وتخزينها والحماية من مخاطرها.
تُؤثّر الحالة الفيزيائيّة للمحروقات، وكلفة نقلها، وقابليتها للإستعمال، على طريقة نقلها وتخزينها.
فالمحروقات الصلبة يمكن نقلها بواسطة البواخر والقطارات والشاحنات في حين أنّ المحروقات السائلة تنقل بالشاحنات التي تحمل الصهاريج، وعن طريق الناقلات العملاقة وعبر خطوط الأنابيب. أمّا المحروقات الغازيّة فتنقل عبر أنابيب الضغط وعبر السفن بعد ان يتمّ إسالتها.
كيفية الوقاية من مخاطر المحروقات
إذا لم تُحترم قواعد السلامة عند نقل المحروقات أو تخزينها أو استعمالها فهذا قد يؤدّي إلى عدّة مخاطر تهدّد الإنسان والبيئة كالإنفجارات وحالات الإختناق والحرائق. لكي نتفادى هذه المخاطر يجب :
← تخزين المحروقات الصلبة في مستودعات خاصّة، وتخزين المحروقات السائلة والغازيّة في خزّانات خاصّة.
← تخزين المحروقات في مكان به تهوئة جيّدة.
← إبعاد مصادر اللهب عن المكان الذي توجد فيه المحروقات
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المادّة في الطبيعة
الذرّة والاحتراق
التفاعل الكيميائي
التحوّل الفيزيائي هو التحوّل الذي لا تتغيّر فيه المادّة من نوع الى آخر، بل يتغيّر شكلها ومظهرها دون أن تتغيّر خواصها (صلبة، سائلة، غازية)،
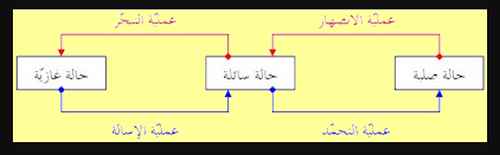
التحوّل الفزيائي
مثال : لو أخذنا قطعة من السكر وتذوّقنا طعمه، ثم وضعناها في كوب من الماء وقلّبناه جيّدا حتى يذوب، ثمّ قمنا بتذوّق ذلك الماء، سنلاحظ أنّ ذوبان السكر في الماء لم يغيّر من طعمه وخواصه.
لكنّ التحوّل الكيميائي هو عبارة عن تغيير في تركيب المادّة ينتج عنه مادّة جديدة تختلف عن المادّة الأولى في خواصها الكيميائيّة والفيزيائيّة. كما تُعرف المواد التي تختفي إثر حصول التفاعل الكيميائي بالمتفاعلات، أمّا المواد التي تظهر إثر حصول التفاعل الكيميائي بمنتجات التفاعل الكيميائي.
مثال :
لو أخذنا قطعة من السكر وتذوّقنا طعمه، ثم وضعناها في ملعقة وجعلناها فوق النار لتسخن، بعد أن تبرد نقوم بتذوّق تلك المادّة التي تكوّنت في الملعقة. سنلاحظ أنّ احتراق السكر ولّد مادّة جديدة لها طعم خاصّ.
مثال :
تحوّل الحديد إلى أكسيد الحديد (الصدأ) في وجود غاز الأكسجين.

ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المادّة في الطبيعة
الذرّة والاحتراق
: الذرّة
⇦ الهباءة هي أصغر جزء ينتج عن تجزئة المادّة ويبقى حاملا لكافة صفاتها.
مثال: أصغر جزء يمكن تسميته سكّر هي هباءة السّكر.
أصغر جزء يمكن تسميته ماء هي هباءة الماء.
تتكوّن كلّ هباءة من عدد معلوم من الجزئيات الصغيرة جدّا يسمّى كلّ منها ذرّة. مثلا: تتكوّن هباءة الماء من ذرّتي هيدروجين وذرّة أكسجين وتتكوّن هباءة الأوزون من ثلاث ذرّات أكسجين.
⇦ تختلف هباءة مادّة ما عن هباءة مادّة أخرى في عدد الذرّات من كلّ نوع.
⇦ الهباءة والذرّة أجسام صغيرة لا ترى بالعين المجرّدة ولا بالمجهر البصري
⇦ تمثّل الذرّات بكويرات بلون وحجم محدّد.
مثال:
تجسّم ذرّة الكربون بكويرة سوداء
تجسّم ذرّة الهيدروجين بكويرة بيضاء
تمثّل هباءة الهيدروجين بكويرتين متلاصقتين
تمثّل هباءة الأوزون بثلاث كويرات متلاصقة

⇦ أثناء التّفاعل الكيميائي تتفكّك كلّ الهباءات وتتجمّع بشكل آخر لتكوّن هباءات جديدة
⇦ يمكن تمثيل التفاعل الكيميائي باعتماد النماذج الهبائيّة
مثال: احتراق الكربون في غاز الأكسجين

⇦ الجسم النقي هو الجسم المكوّن من مادّة واحدة
⇦ الجسم الهبائي النقيّ مكوّن من نوع واحد من الهباءات
⇦ الجسم الهبائي النقي البسيط تتكوّن هباءاته من نوع واحد من الذرّات. كهباءة الأكسجين والتي تتكوّن من ذرّتي أكسجين، وهباءة الأوزون التي تتكوّن من ثلاث ذرّات أكسجين، وهباءة الهيدروجين المتكوّنة من ذرّتي هيدروجين.
⇦ الجسم الهبائي النقيّ المركّب تتكوّن هباءاته من أكثر من نوع من الذرّات. كهباءة الماء التي تتكوّن من ذرّتي هيدروجين وذرّة أكسجين. وهباءة أكسيد الكربون المتكوّنة من ذرّة كربون وذرّتي أكسجين.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المادّة في الطبيعة
الذرّة والاحتراق
بنية الذرة
⇦ تتكوّن الذرّة من نواة وإلكترونات.
⇦ تمثّل شحنة النّواة وكتلتها خاصيّة للذرّة.
⇦ الإلكترونات في حركة دائمة حول النّواة.
الذرّة:
أنواع الذرّة: توجد أنواع متعدّدة من الذرّات.
الشحنة الكهربائيّة للذرّة: صفر.
كتلة الذرة : حوالي
10−26kg
قطر الذرّة: حوالي بضعة أعشار النانومتر
10−10m
النواة:
أنواع النواة: تختلف كلّ نواة ذرّة عن نواة ذرّة أخرى .
الشحنة الكهربائيّة لالنواة: موجبة، وتختلف قيمتها من ذرّة لأخرى.
كتلة النواة: تساوي تقريبا كتلة الذرّة.
قطر النواة: حوالي
15−10m
الإلكترونات:
أنواع الإلكترونات: كلها متطابقة.
الشحنة الكهربائيّة للإلكترونات: سالبة وقيمتها
Qe=−e=−1,6.10−19C
كتلة الإلكترونات:
Me=9,11.10−31kg
ما هي قيمة الشحنة الكهربائيّة:
⇦ قيمة الشحنة الكهربائيّة لمجموع إلكترونات ذرّة واحدة تساوي مقابل قيمة شحنة نواتها يعني:
|إلكتروناتq|=نواةq
مثال: تحتوي ذرّة الهيليوم على إلكترونين:
← شحنة إلكترونين هي:
إلكترونينq=−3,2.10−19C
← شحنة نواة ذرّة الهيليوم هي:
نواةq=3,2.10−19C
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الرموز الكيميائيّة
رمز الذرّة والصيغ الكيميائيّة.
⇦ نرمز للذرّة بالحرف الأوّل من اسمها اللاتيني، مثال:
← ذرّة الكربون رمزها C لأنّ اسمها اللاتيني Carbone
← ذرّة الهيدروجين رمزها H لأنّ اسمها اللاتيني Hydrogène
← ذرّة الكبريت رمزها S لأنّ اسمها اللاتيني Soufre
⇦ وقد نلجأ أحيانا لإضافة حرف ثان لرمز ذرّة، لنميّز بين ذرّتين بدأ اسم كلّ واحد منهما بنفس الحرف. ومثال ذلك:
← رمز ذرّة النحاس Cu، واسمها اللاتيني Cuivre
← رمز ذرّة الكلور Cl، واسمها اللاتيني Chlore
← رمز ذرّة الصوديوم Na، واسمها اللاتيني Soduim (وكان Natrium)
⇦ وتبنى الصيغة الكيميائيّة للهباءة بكتابة رموز الذرّات المكوّنة لها مع إرفاق كلّ رمز على اليمين وفي الأسفل بعدد الذرّات التي يُمثلها في الهباءة (ملاحظة: الرقم 1 لا يكتب في الصيغة الكيميائيّة)
مثال:
← تتكوّن هباءة الأكسجين من ذرّتي أكسجين فصيغتها الكيميائيّة O2
← تتكوّن هباءة الماء من ذرّتي هيدروجين وذرّة أكسجين فصيغتها الكيميائيّة H2O
← تتكوّن هباءة الميتان من ذرّة كربون وأربع ذرّات هيدروجين فصيغتها الكيميائيّة CH4
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الرموز الكيميائية
معادلات التفاعلات الكيميائيّة.
⇦ أثناء كلّ تفاعل كيميائي تُحفظ المادّة. وهذا يعني أنّ مجموع كتلة التفاعلات أصبح مساويا لمجموع كتلة منتجات التفاعل.
مثال: تتفاعل 12g من الكربون مع 32g من الأكسجين لتنتج 44g من ثاني أكسيد الكربون.
⇦ أثناء كلّ تفاعل كيميائي يحفظ العدد الجملي للذرّات من كلّ نوع.
مثال:
كربون غاز الاكسيجين ← كربون غاز الاكسيجين
المتفاعلات ـــــــــــــــــ ذرة كربون منتج التفاعل
ذرة اكسيجين ذرة كربون
ذرة اكسيجين ذرة اكسيجين
⇦ تُكتب معادلة التفاعل الكيميائي باستعمال الرموز والصيغ الكيميائيّة للمتفاعلات ولمنتجات التفاعل.
مثال: احتراق الكربون في غاز الأكسجين يُنتج ثاني أكسيد الكربون.
ومعادلة التفاعل الكيميائي هي:
C + O2 → CO2
⇦ توازن معادلة التفاعل الكيميائي بإضافة عدد صحيح طبيعي يُكتب قبل الصيغة الكيميائيّة لتتساوى عدد الذرّات من كلّ نوع بين المتقابلات ومنتجات التفاعل.
ملاحظة:
← الرقم 1 لا يُكتب في معادلة التفاعل الكيميائي.
← لموازنة معادلة تفاعل كيميائي يمكن ترك العنصر الموجود في جسم نقيّ بسيط للآخر.
C 3 H 8 + O 2 → C O 2 + H 2 O.
الأكسجين موجود في جسم نقي بسيط إذن توازن ذرّات الهيدروجين والكربون ونترك موازنة ذرّات الأكسجين للآخر فنحصل على:
C3H8+5O2→3CO2+H2O
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
ناقليّة المحاليل المائيّة للكهرباء
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
ما هي النواقل:
النّواقل هي الأجسام التي تسمح بمرور الكهرباء عبرها.
الماء النقيّ والتيّار الكهربائي:
الماء النقيّ ناقل للتيّار الكهربائي لكن بصعوبة.
ما هو المحلول المائي الشاردي:
المحلول المائي الشاردي هو المحلول المائي الأقدر من الماء النقيّ على نقل التيّار الكهربائي.
أمثلة لمحاليل مائية شارديّة:
← محلول مائي لكلورير الصوديوم
← محلول مائي للخل
← محلول مائي للصودا.
كيف نتعرّف على محلول مائي شاردي:
للتعرّف على محلول مائي شاردي نقارن ناقليّة هذا المحلول بناقليّة الماء النقي في نفس الظروف.
هام:
← كلّما ارتفعت ناقليّة المحلول المائي كلّما زادت شدّة التيار الكهربائي الذي يعبره.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
تأثير التركيز على ناقليّة المحلول الشاردي للكهربائي
⇦ تتغيّر ناقليّة المحلول المائي الشّاردي حسب طبيعة المنحل وحسب تركيزه.
⇦ كلما ارتفع تركيز محلول مائي شاردي إلاّ وازدادت ناقليّته للتيار الكهربائي.
⇦ كلّما انخفض تركيز محلول مائي شاردي إلاّ وانخفضت ناقليّته للكهرباء.
⇦ يتجلّى لنا تغيّر ناقليّة محلول مائي شاردي في تغيّر قيمة شدّة التيار الكهربائي الذي يعبره.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
الأنيونات والكتيونات
⇦ يحتوي كلّ محلول مائي شاردي على نوعين من الشوارد:
الشوارد الموجبة:
وتسمى كاتيونات، وهي تنتقل في المحلول المائي الشاردي نحو المهبط لذلك تسمّى بالشوارد المهبطيّة. ومثالها: شوارد النحاس. وهي تنتقل في المحلول المائي الشاردي نحو المصعد ولذلك تسمّى بالشوارد المصعديّة. ومثالها: شوارد الكلورير.
⇦ مرور التيّار الكهربائي في محلول مائي شاردي ناتج عن حركة جماعيّة للشوارد.
⇦ إذا ما خسرت أو ربحت ذرّة إلكترون أو أكثر تتحوّل إلى شاردة.
⇦ إذا ما خسرت ذرّة إلكترون أو أكثر تتحوّل إلى شاردة موجبة قيمة شحنتها الكهربائية تساوي قيمة الشحنة الكهربائية البسيطة في عدد الإلكترونات التي خسرتها.
مثال: ذرّة الهيدروجين تخسر إلكترونا واحدا فتتحوّل إلى شاردة هيدروجين وقيمة شحنتها:
q=1×e=1,6.10−19C
⇦ إذا ما رحبت ذرّة إلكترون أو أكثر فإنها تتحوّل إلى شاردة سالبة قيمة شحنتها الكهربائيّة تساوي قيمة شحنة الإلكترونات التي ربحتها
مثال: ذرّة الكلور تربح إلكترونا واحدا فتتحوّل إلى شاردة الكلورير وقيمة شحنتها الكهربائيّة:
q′=1×(−e)=−1,6.10−19C
⇦ المحلول المائي الشاردي متعادل كهربائيّا.
⇦ عند التحوّل من الذرّة إلى الشاردة يتغيّر عدد الإلكترونات، لكن النواة لا تتغيّر وبالتالي نواة الشاردة مطابقة لنواة الذرّة.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
المحلول المائي الحامضي والمحلول المائي القلوي
1) الـpH مقدار عددي يختصّ به كلّ محلول مائي شاردي ويتراوح بين 0 و14 في درجة حرارة تساوي 25°C.
2) قيمة الـpH للماء النقيّ تساوي 7 في درجة حرارة تساوي 25°C.
3) ورق الـpH وجهاز الـpH← متر هي أدوات لقيس pH المحاليل.
4) كلّ محلول مائي شاردي قيمة الـpH لديه أقل من قيمة pH الماء النقي في نفس درجة الحرارة يسمّى محلول حامضي.
مثال: محلول مائي شاردي قيمة الـpH لديه أقل من 7 في درجة حرارة تساوي 25°C هو محلول حامضي.
5) وكلّ محلول مائي شاردي قيمة الـpH لديه أكبر من قيمة pH الماء النقي في نفس درجة الحرارة يُسمّى محلول قلوي.
مثال: محلول مائي شاردي قيمة الـpH لديه أكثر من 7 في درجة حرارة تساوي 25°C هو محلول قلوي.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
محلول PH قيس
1) لقيس pH محلول باستعمال جهاز pH ← متر
أحرصُ على:
← أن يكون الجهاز معيّرا.
← أن تشطّف مسبر الجهاز بالماء المقطّر، ثمّ تجفّفه إثر كلّ عمليّة قيس.
← أن تغمّس كامل الجزء الحسّاس للمسبر في المحلول دون أن يلمس طرفه السفلي قاع الإناء.
2) الـpH ← متر جهاز قيس دقيق.
3) عند قيس pH محلول باستعمال ورق الـpH أقارنُ الألوان الظاهرة على قطعة الشريط المبلّل بالمحلول مع ألوان الدليل المرسومة على علبة ورق الـpH المستعمل.
4) ورق الـpH أداة قيس عمليّة، لكنّها غير دقيقة.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
درجة حموضة محلول مائي حامضي
⇦ كلّ محلول حامضي له درجة حموضة معيّنة.
مثال: قروصة مذاق محلول مائي لعصير الليمون تمثّل درجة لحموضة المحلول.
⇦ كلّما ازداد تركيز محلول مائي حامضي إلاّ وازدادت درجة حموضته والعكس بالعكس.
مثال: كلّما ازداد تركيز محلول مائي لعصير الليمون إلاّ وازدادت قروصته وبالتالي حموضته.
هام:
← عندما تزداد درجة حموضة محلول مائي شاردي تنخفض قيمة pH المحلول.
← عندما تنخفض قيمة pH محلول مائي شاردي ترتفع درجة حموضة المحلول.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشارديّة
درجة قلويّة محلول مائي قلوي
⇦ لكلّ محلول قلوي درجة قلويّة معيّنة.
مثال: مرارة مذاق محلول مائي لخميرة الطعام تمثّل درجة قلويّة المحلول.
⇦ كلّما ازداد تركيز محلول مائي قلوي إلاّ وازدادت درجة قلويّته.
مثال: كلّما ازداد تركيز محلول مائي لخميرة الطّعام إلاّ وازدادت مرارته وبالتالي درجة قلويّته.
هام:
← عندما تزداد درجة قلويّة محلول مائي شاردي ترتفع قيمة الـpH لديه.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
المحاليل الشاردية
المحلول المتعادل
⇦ المحلول متعادل هو كل محلول مائي شاردي قيمة الـpH لديه تساوي قيمة pH الماء النقي في نفس درجة الحرارة.
مثال: pH محلول مائي لملح الطعام يساوي 7 في 25°C.
المحلول المائي لملح الطّعام هو محلول متعادل.
⇦ للمحاليل المتعادلة استعمالات عدّة في حياتنا اليوميّة.
مثال: الشمبوهات المخصّصة أساسا للرضّع والأطفال هي بالأساس محاليل متعادلة أو قليلة الحموضة في أغلبها.
هام:
لا تتغيّر طبيعة محلول مائي متعادل عندما نغيّر تركيزه أو نغيّر درجة حرارته.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الضوء
تغيير مسار الضوء
انعكاس الضوء
⇦ إنّ انعكاس الضّوء هو ارتداد الضّوء في منحى معيّن دون غيره على مستوى سطح صقيل. وارتداده يعني تغيّر مساره مع بقائه في نفس الوسط البصري.
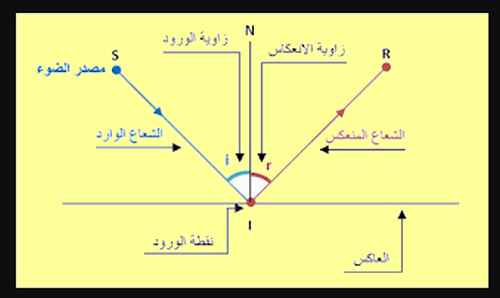
⇦ السّطح الصّقيل أو العاكس هو السّطح الذي يحدث على مستواه انعكاس الضوء.
⇦ الشعاع الوارد SI
هو الشعاع المنطلق من مصدر الضوء S
والمتجه نحو نقطة الورود I
.
⇦ الشعاع المنعكس IR
هو الشعاع المرتدّ على مستوى العاكس.
⇦ زاوية الورود i
هي زاوية ناتجة عن تقاطع الشعاع الوارد SI
مع العمود القائم IN
على العاكس.
⇦ زاوية الانعكاس r
هي زاوية ناتجة عن تقاطع الشعاع المنعكس IR
مع العمود القائم IN
على العاكس.
⇦ مستوي الورود هو المستوي الذي يحوي العمود القائم IN
على العاكس والشعاع الوارد SI
.
قانونا انعكاس الضوء:
⇦ قانون المستويات:
ينتشر الشعاع المنعكس في مستوي الورود.
⇦ قانون الزوايا:
قيمة زاوية الانعكاس تساوي قيمة زاوية الورود i=r
.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الضوء
تغيير مسار الضوء
المرآة المسطّحة
كلّ جسم حقيقي له صورة افتراضيّة عبر مرآة مسطّحة، وهي متناظرة معه بالنسبة لمستوى المرآة.
⇦ يكون رسم صورة جسم حقيقي S
عبر مرآة مسطّحة بالاعتماد على قانوني الانعكاس كالتالي:
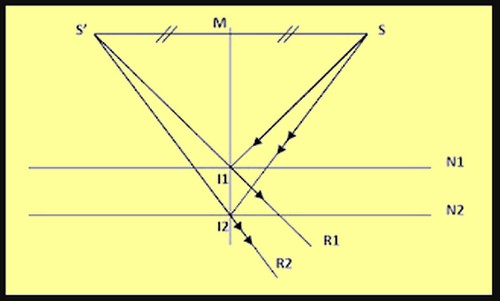
المرآة المسطّحة ← الموسوعة المدرسية
⇦ الصورة الافتراضية ′S
تنتج عن تقاطع امتداد الأشعة I1R1
أو I2R2
.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الضوء
تغيير مسار الضوء
انكسار الضوء
انكسار الضوء هو تغيّر مساره عند مروره من وسط شفّاف إلى وسط شفّاف آخر. ومثال ذلك:
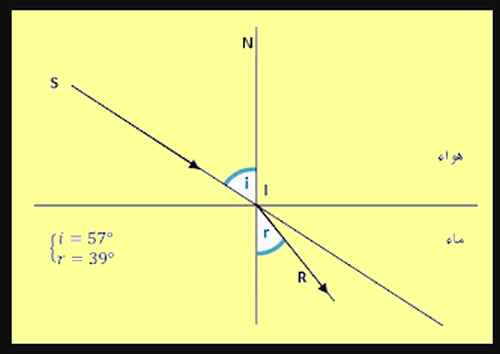
← الشّعاع الوارد SI
هو الشعاع المنطلق من مصدر الضوء S
والمتجه نحو نقطة الورود I
.
← الشعاع المنكسر IR
هو الشعاع المنعطف في مستوى السطح الفاصل بين والسطين الشفافين.
← زاوية الورود i
هي زاوية ناتجة عن تقاطع الشعاع الوارد SI
مع العمود القائم IN
على السطح الفاصل بين الوسطين الشفافين.
← زاوية الانكسار r
هي زاوية ناتجة عن تقاطع الشعاع المنكسر IR
مع العمود القائم IN
على السطح الفاصل بين الوسطين الشفافين.
قانونا انكسار الضوء:
← قانون المستويات:
ينتشر الشعاع المنكسر في مستوى الورود.
← قانون الزوايا:
في كل انكسار للضوء ينتج عن مروره من الهواء إلى وسط شفاف آخر ينعطف الشعاع المنكسر نحو العمود القائم على السطح الفاصل بين الوسطين بحدة مرتبطة بانكساريّة ذلك الوسط وبالتالي تكون قيمة زاوية الانكسار أصغر من قيمة زاوية الورود.
⇦ الانكساريّة تميّز حدّة انحراف الضوء في وسط بصري معيّن.
مثال:
وبالتالي نقول إنّ انكساريّة البلاكسيقلاس أكبر من انكساريّة الماء
⇦ عند مرور الضوء من الهواء إلى وسط شفاف آخر إذا بلغت زاوية الورود قيمتها القصوى 90∘
تكون زاوية الانكسار قصوى ورمزها
λ
وهي تميّزه عن غيره
i=90∘⇒r=λ
هام:
← لا يحدث انكسار للضّوء الوارد عندما تساوي قيمة زاوية الورود صفر درجة.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الضوء
تغيير مسار الضوء
الانكسار الحدّي والانعكاس الكلّي
⇦ عند انكسار الضّوء نتيجة مروره من وسط شفّاف إلى الهواء ينعطف الشّعاع الضوئي نحو السّطح الفاصل بين الوسطين بحدّة مرتبطة بانكساريّة ذلك الوسط وبالتالي تكون قيمة زاوية الانكسار أكبر من قيمة زاوية الورود
مثال:
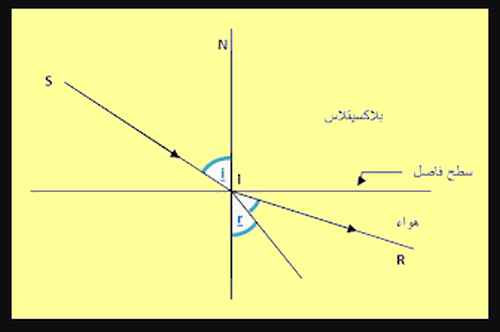
⇦ عندما تكون قيمة زاوية الورود i
مساوية لقيمة الزاوية λ
تكون قيمة زاوية الانكسار 90∘
وبذلك يكون الشّعاع المنكسر مماسا للسطح الفاصل بين الوسطين. تسمّى هذه الظّاهرة بالانكسار الحدّي.
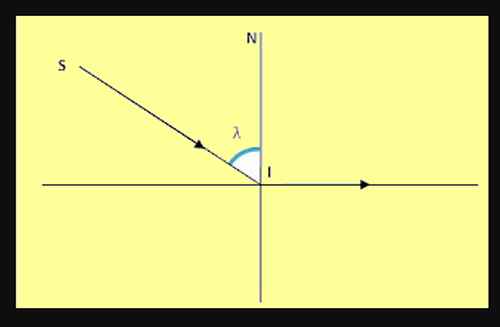
تسمّى λ
زاوية الورود الحرجة
⇦ لا يحدث انكسار الضّوء المار من وسط شفّاف إلى الهواء عندما تتجاوز قيمة زاوية الورود قيمة الزاوية الحرجة λ
لكن يحدث انعكاس كلّي للشعاع الوارد على مستوى السّطح الفاصل.
هام:
← لا يحدث انكسار للضّوء عندما تساوي قيمة زاوية الورود صفر درجة ويمرّ الشعاع من الوسط الشفاف إلى الهواء دون تغيير مساره
ملاحظة:
← عند ورود شعاع ضوئي على سطح صقيل فاصل بين وسطين شفافين يمكن أن تحدث له ظاهرة الانكسار والانعكاس معا.
← قيمة الزاوية الحرجة λ
تساوي قيمة زاوية الانكسار القصوى.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الضوء
تغيير مسار الضوء
تطبيقات لتغيّر مسار الضوء
من تطبيقات الانكسار الحدّي والانعكاس الكلّي للضوء الألياف البصريّة والسّراب.
1) الألياف البصريّة:
← تستعمل الليفة البصريّة، للنقل الموجّه والدقيق للإشارات الضوئيّة في مجال الاتصالات والمجال الطبّي مثلا. وهي تتكوّن أساسا من خيط زجاجي، ذي انكساريّة مرتفعة، يُسمّى قلب الليفة، ويلفّه غشاء من زجاج آخر أقل انكساريّة، يُسمّى الغلاف البصري.
← ينتشر الضوء في قلب الليفة حيث يرِد على السطح الفاصل بين القلب والغلاف البصري تحت زاوية ورود أكبر من قيمة الزاوية الحرجة λ
، فيلعب هذا الأخير دور المرآة، ليعكس كليّا الضوء. وهكذا تتالى الانعكاسات الكليّة للضوء حتّى يعبر كامل الليفة.
2) السّراب:
السّراب، ظاهرة طبيعيّة تتمثّل في مشاهدة برك ماء وهميّة، على مسافة بعيدة في طقس شديد الحرارة. وتحدث بسبب الاختلاف في انكساريّة طبقات الهواء، حيث تنخفض انكساريّة الهواء القريب من سطح الأرض، عندما ترتفع درجة الحرارة. فيحدث انعكاس كلّي لضوء صادر عن جسم ما على مستوى سطح إحدى هذه الطّبقات.
هام: هناك سراب قطبي يحدث عندما تنخفض درجة الحرارة، إذ أنّ انكساريّة الهواء ترتفع بانخفاض درجة حرارة الهواء.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الضوء
تغيير مسار الضوء
← الموشور هو وسط شفّاف، متجانس، يحدّه وجهان مستويان يتقاطعان عند مستقيم يسمّى حرف الموشور، ويُسمّى بقاعدة الموشور، الوجه المقابل لحرف الموشور.
الموشور
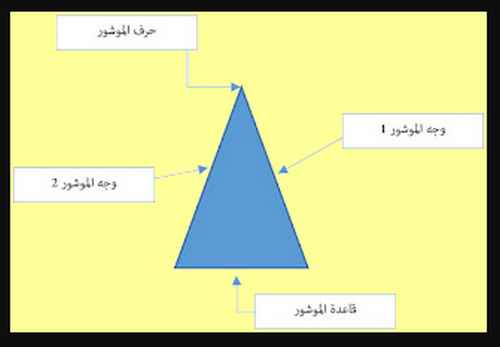
← عند مرور شعاع ضوئي عبر موشور، فإنّه ينكسر مرّة أولى في النقطة I1 ثمّ ينكسر مرّة ثانية في النقطة I2 ليخرج إلى الهواء.
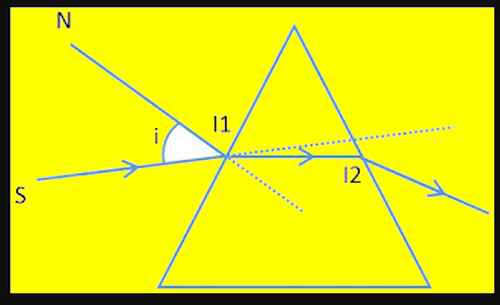
مرور شعاع ضوئي عبر موشور
ملاحظة:
يمكن أن يحدث للشّعاع I1I2 انعكاس كلّي في النّقطة I2 حسب قيمة زاوية الورود، والموشور المستعمل.
← عندما نستعمل مصدرا للضّوء الأبيض، نشاهد على الشّاشة بقعة ضوئيّة تندرج فيها الألوان بدون انقطاع من الأحمر إلى البنفسجي، وتسمّى طيف الضّوء الأبيض ونقول أنّ هذا الأخير تشتّت.
← كلّ لون يظهر على الشّاشة يميّز إشعاعه أحاديّة اللّون حصل لها انحراف في مسارها بقيمة معيّنة ترتفع من الأحمر إلى البنفسجي مرورا بالبرتقالي فالأصفر فالأخضر فالأزرق فالنيلي.
← للضّوء الأبيض طيف يُميّزه عن غيره من الأضواء.
← الضوء الصادر عن تأجّج سليك مصباح يعتبر ضوء أبيضا أمّا الضوء الصادر عن مصدر ليزر فلا يُعتبر كذلك، لأنّ طيفه لا يتطابق مع طيف الضوء الأبيض.
← ظاهرة قوس فزح تنتج عن تشتّت الضوء الأبيض المنبعث من الشمس عبر قطرات الماء العالقة في الجوّ، وتُشاهد غالبا بعد نزول الأمطار.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الطاقة الضوئيّة
مفهوم الطاقة الضوئيّة.
يتم تحويل الطاقة الضوئية إلى أنواع أخرى من الطاقة وذلك حسب الحاجة المراد بها، مثل الطاقة الكهربائية في الخلايا الضوئية، أو الطاقة الحرارية في عمليات التسخين الحراري كما هو الحال في تسخين المياه والسوائل الأخرى. ويستخدم النبات الطاقة الضوئية مباشرة لعمليات التمثيل البنائي لإنتاج مركبات عضوية تختزن طاقة كيميائية.
والطاقة الضوئية هي عبارة عن موجات كهرومغناطيسية تحتوي كل منها على حزم من الفوتونات، وتختلف الموجات الكهرومغناطيسية في خواصها الفيزيائية باختلاف الأطوال الموجية، فمثلاً نجد أن الموجات ذات الطول الموجي الذي يتراوح بين عدة كيلومترات إلى عدة سنتيمترات يستخدم في الدوائر الإلكترونية ومحطات الإرسال والاستقبال التلفزيوني. وتتميز الأشعة السينية x←ray وأشعة جاما بتردد عالي جداً وبالتالي تكون ذات طاقة عالية لها القدرة على النفاذ خلال الأوساط المادية.
الأشعة السينية
وهي عبارة عن أشعة غير مرئية ذات طول موجي قصير جداً، وتستخدم في المجال الطبي وكذلك في دراسة البلورات لمعرفة خصائصها.
أشعة جاما
وهي عبارة عن أشعة لا تتأثر بالمجالات الكهربية أو المغناطيسية ولها القدرة على النفاذ وهي تعتبر من الأشعة الخطرة.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
الطاقة الضوئيّة
الطاقة الشمسيّة.
الطاقة الشمسية هي مصدر للطاقة لا ينضب ولكنها تصل إلينا بشكل مبعثر إذ يبلغ منها حوالي 70% تقريبا وذلك بسبب الإشعاع أو الانعكاس.
والطاقة الشمسية طاقة نظيفة فلا ينتج عن استعمالها غازات أو نواتج ضارة بالبيئة كما هي الحال في أنواع الوقود التقليدي.
إن استعمال الطاقة الشمسية حل جذري لمشكل الإستهلاك المتزايد للطاقة كل يوم حيث أنها مصدر متجدد لا يمكن أن نفقده يوما ما وقد تم إنشاء أكبر محطة للطاقة الشمسية في العالم وذلك بالمغرب و بالضبط بمدينة ورززات .
تحميل كتاب العلوم الفيزيائية 9 اساسي من هنا







